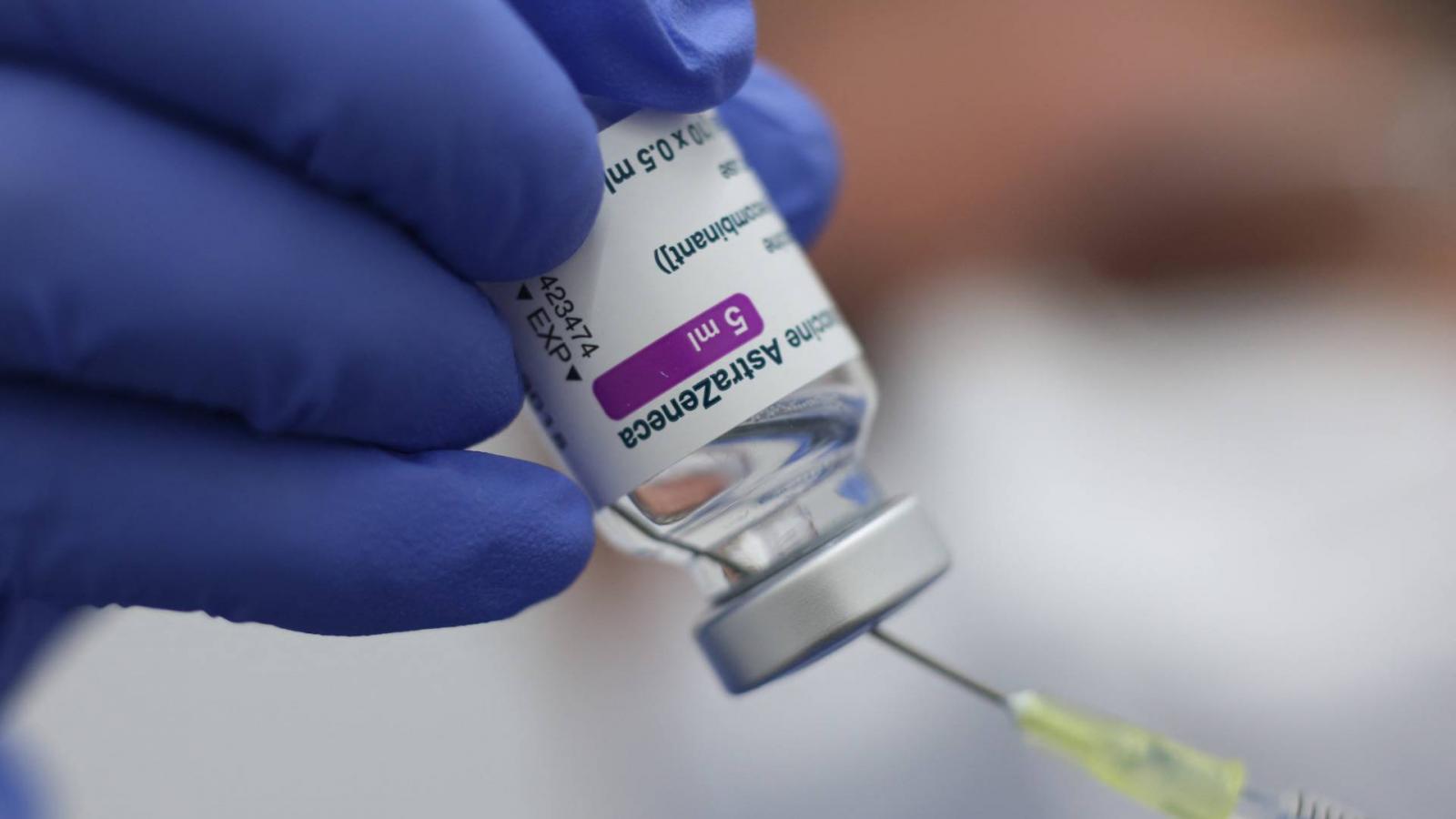
Az Európai Gyógyszerügynökség (EMA) szerint van összefüggés a nagyon ritkán kialakuló vérrögképződés és az AstraZeneca által gyártott Covid-19 ellenes oltóanyag között. Ugyanakkor az EU gyógyszerfelügyeleti hatóságának szerepét betöltő hivatal nem változtatott eddigi iránymutatásain, és továbbra is kitart amellett, hogy a vakcina előnyei felülmúlják a lehetséges kockázatait. Az EMA nem adott ki ajánlást a készítmény használatának korlátozására sem. Emer Cooke ügyvezető igazgató ugyanakkor bejelentette, hogy tovább vizsgálják az Európában engedélyezett oltóanyagok biztonságosságát és hatékonyságát a folyamatosan beérkező adatok alapján, és ha szükséges, újabb javaslatokat tesznek.
Az uniós országok egészségügyi miniszterei szerda esti virtuális tanácskozáson egyeztettek a további lépésekről.
Az európai gyógyszerhatóság 62 agyi vénás trombózisos és 24 zsigeri vénás trombózisos esetet vizsgált, amelyek közül 18 végződött halállal. A megbetegedés főleg 60 év alatti nők körében jelentkezett az oltást követő két hétben. Az EMA szerint egyelőre kevés adat áll rendelkezésre annak a megállapításához, hogy a ritka mellékhatások pontosan mely korcsoportokat és betegeket veszélyeztetnek a leginkább.
Márciusban összesen 16 európai ország vezetett be kisebb-nagyobb korlátozásokat az AstraZeneca használatára a rendkívül ritkán előforduló vérrögképződés miatt. Az EMA március végén közzétett kedvező véleményét követően a tagállamok zöme feloldotta a szigorítást. Ekkor a hatóság azt állította, hogy nem lát bizonyítható összefüggést a vakcina és a véralvadássál kapcsolatos, kisszámú eset között. Azóta újabb trombózisos esetek történtek, amelyek ismét óvatosságra intették a védőoltás alkalmazóit.
Az Európai Gyógyszerügynökség ajánlásával szemben szerdán a brit gyógyszerhatóság arra figyelmeztetett, hogy a szigetországban fel kell függeszteni az AstraZeneca készítményének a használatát a 18-29 éves korosztály számára.
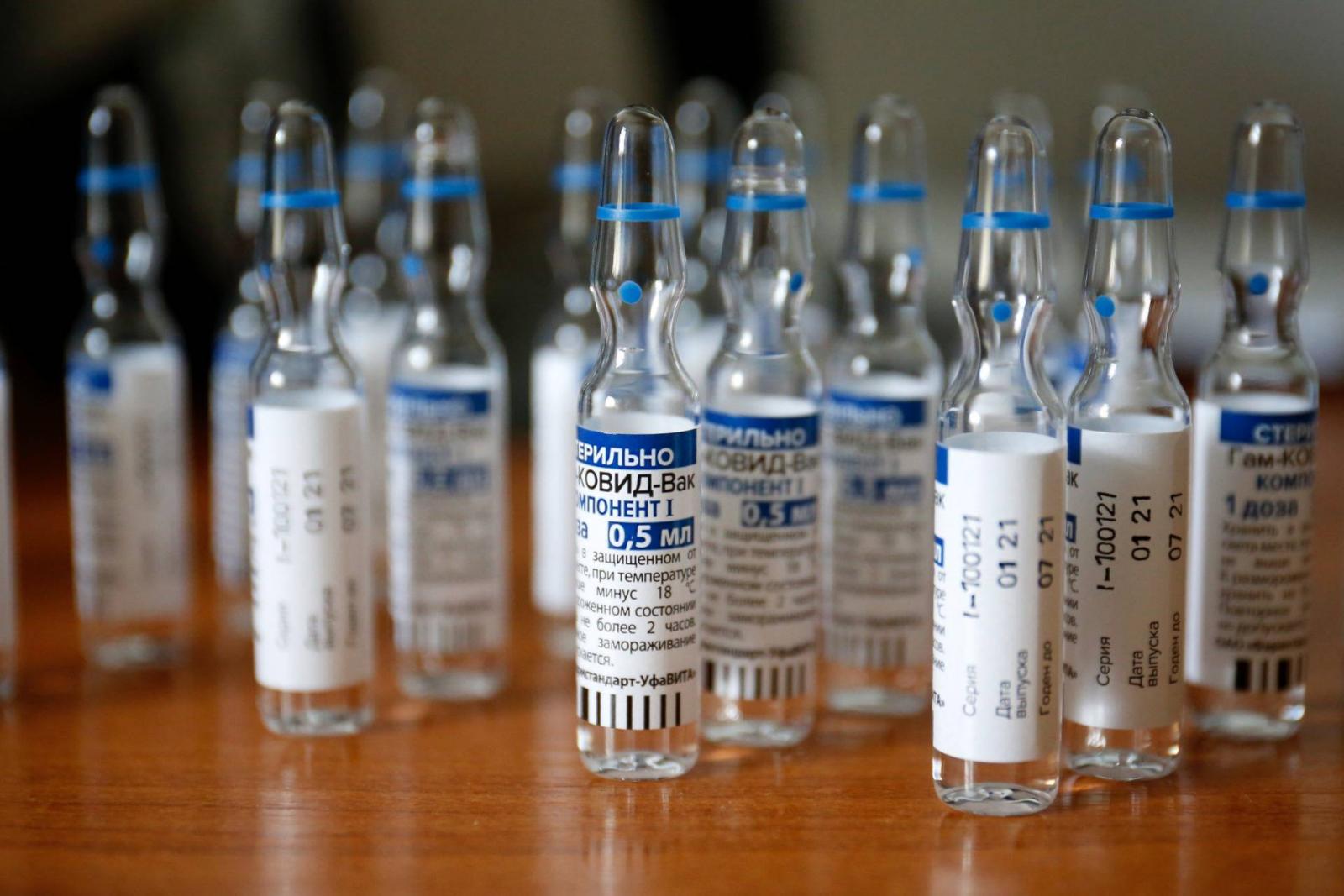
Az EMA a jövő héten vizsgálatot kezd annak megállapítására, hogy az orosz Szputnyik V vakcina klinikai tesztvizsgálatai megfeleltek-e a nemzetközileg elfogadott etikai és tudományos előírásoknak. Emer Cooke ügyvezető igazgató megerősítette a Financial Times című brit lap információit, amelyek szerint a hatóság annak kíván a helyszínen utánajárni, hogy az oltóanyag biztonságosságát és hatásosságát mérő oroszországi vizsgálatok összhangban voltak és vannak-e a „helyes klinikai gyakorlat” normáival. Ezek olyan nemzetközileg elfogadott követelmények, amelyeknek betartása biztosítja, hogy a klinikai vizsgálatba bevont személyek jogai, biztonsága és jóléte megfelelő védelemben részesül, és hogy a vizsgálat megfelelő adatokat szolgáltat.
Az oroszok állítása szerint a vakcina klinikai tesztelését egy állami laboratóriumban végezték, és a vizsgálatokban katonák, valamint állami alkalmazottak vettek részt. A Reuters hírügynökség arról írt, hogy néhány résztvevő azt állította: a felettese nyomására jelentkezett.
Kirill Dmitrijev, a Szputnyik V fejlesztését finanszírozó állami vagyonalap vezetője cáfolta, hogy kényszert alkalmaztak volna, szerinte senkire nem gyakoroltak nyomást, az oltóanyag bevizsgálása során tiszteletben tartottak minden nemzetközi előírást. Azt állította, hogy nincs tudomása az EMA aggodalmairól, a “kiszivárogtatás” pedig csak azt a célt szolgálja, hogy “aláássa” az európai engedélyezési folyamatot.
Az Európai Gyógyszerügynökség jelenleg tanulmányozza a Szputnyik V vakcinát, és a jóváhagyását attól teszi függővé, hogy az elvégzett klinikai vizsgálatok megfeleltek-e a “helyes klinikai gyakorlat” nemzetközi szabványainak. Az EMA illetékese azt nyilatkozta a brit lapnak, hogy amennyiben az aggodalmaik beigazolódnak, további ellenőrzésekre lesz szükség, de részletekkel nem szolgált.
Ettől függetlenül kerül sor az európai hatóság szakértőinek jövő hónapra tervezett oroszországi gyárlátogatására, amit azonban néhány nappal elhalasztottak. A vendéglátók ugyanis nem tudnak egyszerre annyi külföldi ellenőrt fogadni, mint ahányan meg akarják látogatni a vakcinát előállító üzemet. Kirill Dmitrijev szerint elsőbbséget adnak azoknak, akik már kötelezettséget vállaltak, hogy vásárolnak az oltóanyagból, és az Európai Bizottság nincs ezek között.
Az Európai Unió országai közül eddig Magyarország és Szlovákia vásárolt az orosz vakcinából. A két ország vészhelyzeti eljárás keretében döntött az EU-ban még nem engedélyezett készítmény beszerzéséről.
Időközben Szlovákiában is problémák merültek fel a Szputnyik V használatával kapcsolatban. Kiderült, hogy a leszállított készítmény nem azonos azzal, amiről a brit Lancet folyóirat azt állította, hogy 90 százalék fölötti a hatékonysága. Az ország 200 ezer adag Szputnyikot vásárolt, de egyelőre nem oltanak vele. A Dennik N című lap szerint további dokumentációra várnak a gyártótól, az egészségügyi miniszter a szlovák gyógyszerhatóság ajánlásainak fényében dönt majd a vakcina további sorsáról, várhatóan a jövő héten.